Идеал газ, идеалдуу газ абалынын теңдемеси, анын температурасы жана басымы, көлөмү… физиканын тиешелүү бөлүмүндө колдонулган параметрлердин жана аныктамалардын тизмесин бир топ убакытка чейин улантууга болот. Бүгүн биз ушул темада сүйлөшөбүз.
Молекулярдык физикада эмне каралат?

Бул бөлүмдө каралган негизги объект идеалдуу газ болуп саналат. Идеалдуу газ абалынын теңдемеси экологиянын нормалдуу шарттарын эске алуу менен алынган жана бул тууралуу бир аз кийинчерээк сүйлөшөбүз. Эми бул "көйгөйгө" алыстан кайрылалы.
Бир аз газ массасы бар дейли. Анын абалын термодинамикалык мүнөздөгү үч параметр аркылуу аныктоого болот. Булар, албетте, басым, көлөм жана температура. Бул учурда системанын абалынын теңдемеси тиешелүү параметрлердин ортосундагы байланыштын формуласы болот. Бул төмөнкүдөй көрүнөт: F (p, V, T)=0.
Бул жерде биз биринчи жолу идеалдуу нерсенин пайда болушуна акырындап жакындап жатабызгаз. Ал молекулалардын ортосундагы өз ара аракеттешүү анчалык деле байкалбаган газ деп аталат. Жалпысынан алганда, бул жаратылышта жок. Бирок, кандай гана болбосун өтө сейрек кездешүүчү газ ага жакын. Кадимки шарттарда болгон азот, кычкылтек жана аба идеалдан анча айырмаланбайт. Идеал газдын абалынын теңдемесин жазуу үчүн бирдиктүү газ мыйзамын колдонсок болот. Биз алабыз: pV/T=const.
Байланыштуу түшүнүк №1: Авогадро мыйзамы
Ал бизге айта алат, эгерде биз абсолюттук кандайдыр бир туш келди газдын бирдей сандагы молдорун алып, аларды бирдей шарттарга, анын ичинде температура менен басымга койсок, анда газдар бирдей көлөмдү ээлейт. Атап айтканда, эксперимент нормалдуу шарттарда жургузулду. Бул температура 273,15 Kelvin, басымы бир атмосфера (760 миллиметр сымап, же 101325 Паскаль) болгон дегенди билдирет. Бул параметрлер менен газ 22,4 литрге барабар көлөмүн ээлеген. Демек, кандайдыр бир газдын бир моль үчүн сандык параметрлердин катышы туруктуу мааниге ээ болот деп айта алабыз. Мына ошондуктан бул фигураны R тамгасы менен белгилөө жана аны универсалдуу газ константасы деп атоо чечими кабыл алынган. Ошентип, ал 8,31ге барабар. Дж/мольК.
Идеалдуу газ. Идеалдуу газ абалынын теңдемеси жана аны манипуляциялоо
Формуланы кайра жазганга аракет кылалы. Бул үчүн, биз аны төмөнкү формада жазабыз: pV=RT. Андан кийин, биз жөнөкөй иш-аракет жасайбыз, теңдеменин эки тарабын каалаган моль санына көбөйтөбүз. Биз pVu=uRT алабыз. молярдык көлөмдүн көбөйтүлгөнүн эске алалы жаназаттын көлөмү жөн гана көлөмү. Бирок, баары бир, моль саны бир эле учурда масса жана молярдык масса менен барабар болот. Менделеев-Клапейрон теңдемеси дал ушундай көрүнөт. Бул идеалдуу газдын кандай система түзөрү жөнүндө так түшүнүк берет. Идеалдуу газдын абалынын теңдемеси төмөнкү формада болот: pV=mRT/M.
Басымдын формуласын чыгаргыла
Алынган туюнтмалар менен дагы бир нече манипуляцияларды жасайлы. Бул үчүн Менделеев-Клапейрон теңдемесинин оң тарабы Авогадро санына көбөйтүлөт жана бөлүнөт. Эми биз Авогадро саны боюнча заттын көлөмүнүн көбөйтүлүшүнө кылдаттык менен карайбыз. Бул газдагы молекулалардын жалпы санынан башка эч нерсе эмес. Бирок ошол эле учурда универсалдуу газ константасынын Авогадро санына болгон катышы Больцман туруктуусуна барабар болот. Демек, басымдын формулаларын төмөнкүчө жазууга болот: p=NkT/V же p=nkT. Бул жерде n символу бөлүкчөлөрдүн концентрациясы.
Идеалдуу газ процесстери
Молекулярдык физикада изопроцесстер деген нерсе бар. Бул системада туруктуу параметрлердин биринде жүрүп жаткан термодинамикалык процесстер. Бул учурда заттын массасы да туруктуу болушу керек. Келгиле, аларга көбүрөөк токтололу. Демек, идеалдуу газдын мыйзамдары.
Басым туруктуу бойдон калат
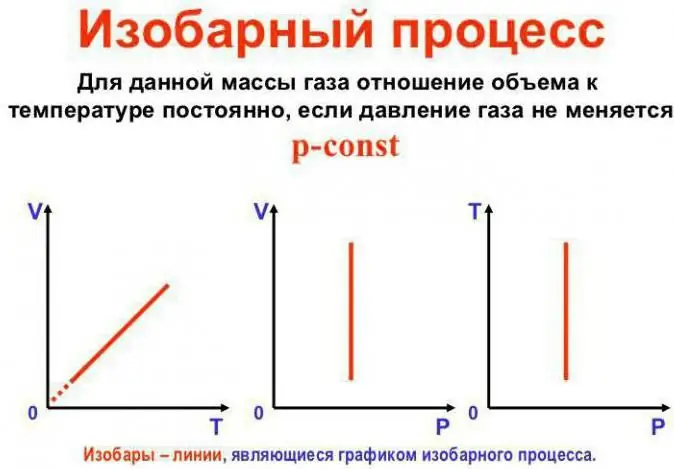
Бул Гей-Люссактын мыйзамы. Бул төмөнкүдөй көрүнөт: V/T=const. Аны башка жол менен кайра жазууга болот: V=Vo (1 + at). Бул жерде a 1/273,15 К^-1ге барабар жана "көлөмдүн кеңейүү коэффициенти" деп аталат. Температураны Цельсий боюнча да алмаштыра алабызКелвин шкаласы. Акыркы учурда V=Voat формуласын алабыз.
Үнү өзгөрүүсүз калат

Бул Гей-Люссактын экинчи мыйзамы, көбүнчө Чарльздын мыйзамы деп аталат. Бул төмөнкүдөй көрүнөт: p/T=const. Дагы бир формула бар: p=po (1 + at). Трансформациялар мурунку мисалга ылайык жүргүзүлүшү мүмкүн. Көрүнүп тургандай, идеалдуу газ мыйзамдары кээде бири-бирине абдан окшош.
Температура туруктуу бойдон калат

Эгер идеалдуу газдын температурасы туруктуу болсо, анда Бойль-Мариотт мыйзамын алабыз. Муну төмөнкүчө жазса болот: pV=const.
Байланыштуу түшүнүк №2: Жарым-жартылай басым
Бизде газдар бар идиш бар дейли. Бул аралашма болот. Система жылуулук тең салмактуулук абалында, ал эми газдар бири-бири менен реакцияга кирбейт. Бул жерде N молекулалардын жалпы санын билдирет. N1, N2 жана башкалар, тиешелүүлүгүнө жараша, аралашма компоненттеринин ар бириндеги молекулалардын саны. p=nkT=NkT/V басым формуласын алалы. Аны белгилүү бир иш үчүн ачууга болот. Эки компоненттүү аралашма үчүн формула төмөнкүдөй формада болот: p=(N1 + N2) kT/V. Бирок андан кийин ар бир аралашманын жарым-жартылай басымынан жалпы басым чыгарылат экен. Ошентип, ал p1 + p2 жана башкалар сыяктуу болот. Бул жарым-жартылай басымдар болот.
Бул эмне үчүн?
Биз алган формула системадагы басымдын ар бир молекула тобунан экенин көрсөтүп турат. Баса, бул көз каранды эмесбашкалар. Далтон мыйзамды түзүүдө ушундан пайдаланган, кийинчерээк анын аты менен аталган: газдар бири-бири менен химиялык реакцияга кирбеген аралашмада жалпы басым жарым-жартылай басымдардын суммасына барабар болот.






