Термодинамиканын маанилүү бөлүмү заттын ар кандай фазаларынын ортосундагы өзгөрүүнү изилдөө болуп саналат, анткени бул процесстер практикада жүрөт жана белгилүү бир шарттарда системанын жүрүм-турумун алдын ала айтуу үчүн принципиалдуу мааниге ээ. Бул трансформациялар макала арналган фазалык өтүү деп аталат.
Фаза жана системалык компонент түшүнүгү

Физикада фазалык өтүүлөрдү кароого өтүүдөн мурун фазанын өзүнүн түшүнүгүн аныктоо зарыл. Жалпы физика курсунан белгилүү болгондой, заттын үч абалы бар: газ, катуу жана суюк. Илимдин өзгөчө бөлүмүндө - термодинамикада мыйзамдар алардын агрегаттык абалдары үчүн эмес, материянын фазалары үчүн түзүлгөн. Фаза деп бир тектүү түзүлүшкө ээ, спецификалык физикалык жана химиялык касиеттери менен мүнөздөлгөн жана материянын калган бөлүгүнөн интерфаза деп аталган чектер менен бөлүнгөн материянын белгилүү бир көлөмү түшүнүлөт.
Ошентип, "фаза" түшүнүгү касиеттери жөнүндө практикалык жактан алда канча маанилүү маалыматты камтыйт.анын агрегаттык абалына караганда. Мисалы, темир сыяктуу металлдын катуу абалы төмөнкү фазаларда болушу мүмкүн: төмөнкү температурадагы магниттик дене-центрлүү куб (BCC), төмөнкү температурадагы магниттик эмес bcc, бет-борбордук куб (fcc) жана жогорку- температура магниттик эмес Bcc.
Термодинамика мыйзамдарында «фаза» түшүнүгүнөн тышкары «компоненттер» термини да колдонулат, бул белгилүү бир системаны түзгөн химиялык элементтердин санын билдирет. Бул фаза монокомпоненттүү (1 химиялык элемент) же көп компоненттүү (бир нече химиялык элементтер) болушу мүмкүн экенин билдирет.
Гиббс теоремасы жана системанын фазаларынын ортосундагы тең салмактуулук

Фазалык өтүүлөрдү түшүнүү үчүн алардын ортосундагы тең салмактуулук шарттарын билүү зарыл. Бул шарттарды математикалык жол менен алардын ар бири үчүн Гиббс теңдемелеринин системасын чечүү жолу менен алууга болот, муну менен тең салмактуулук абалга тышкы таасирден обочолонгон системанын жалпы Гиббс энергиясы өзгөрүүсү токтогондо жетет.
Белгиленген теңдемелер системасын чечүүнүн натыйжасында бир нече фазалардын ортосунда тең салмактуулуктун болушу үчүн шарттар түзүлөт: изоляцияланган система басым, ар бир компоненттин химиялык потенциалы жана бардык фазаларда температура болгондо гана эволюциясын токтотот. бири-бирине барабар.
Тең салмактуулук үчүн Гиббс фазасынын эрежеси

Бир нече фазалардан жана компоненттерден турган система тең салмактуулукта гана эмесбелгилүү бир шарттарда, мисалы, белгилүү бир температурада жана басымда. Тең салмактуулук үчүн Гиббс теоремасындагы кээ бир өзгөрмөлөр фазалардын санын да, бул тең салмактуулукта турган компоненттердин санын да сактоо менен өзгөртүлүшү мүмкүн. Системадагы тең салмактуулукту бузбастан өзгөртүүгө боло турган өзгөрмөлөрдүн саны бул системанын эркиндиктеринин саны деп аталат.
f фазалардан жана k компоненттен турган системанын l эркиндиктеринин саны Гиббс фазасынын эрежеси боюнча өзгөчө аныкталат. Бул эреже математикалык түрдө төмөнкүчө жазылган: l + f=k + 2. Бул эреже менен кантип иштөө керек? Өтө жөнөкөй. Мисалы, система f=3 тең салмактуулук фазасынан турганы белгилүү. Мындай система камтышы мүмкүн болгон компоненттердин минималдуу саны канча? Суроого төмөнкүдөй ой жүгүртүү менен жооп бере аласыз: тең салмактуулукта эң катаал шарттар ал белгилүү бир көрсөткүчтөр боюнча гана ишке ашканда болот, башкача айтканда, кандайдыр бир термодинамикалык параметрдин өзгөрүшү дисбаланска алып келет. Бул эркиндиктердин саны l=0 дегенди билдирет. Белгилүү l жана f маанилерин алмаштыруу менен k=1 алабыз, башкача айтканда үч фаза тең салмактуулукта турган система бир компоненттен турушу мүмкүн. Мында муз, суюк суу жана буу белгилүү температурада жана басымда тең салмактуулукта турган суунун үчтүк чекити эң сонун мисал.
Фазалык трансформациялардын классификациясы
Эгер сиз тең салмактуулуктагы системанын кээ бир термодинамикалык параметрлерин өзгөртө баштасаңыз, бир фаза кантип жоголуп, экинчиси пайда болоорун байкай аласыз. Бул процесстин жөнөкөй мисалы - муздун ысытылганда эриши.
Гиббс теңдемеси эки өзгөрмөгө (басым жана температура) гана көз каранды экенин жана фазалык өтүү бул өзгөрмөлөрдүн өзгөрүшүн камтый турганын эске алсак, анда математикалык түрдө фазалардын ортосундагы өтүүнү Гиббс энергиясын анын энергиясына карата дифференциациялоо менен сүрөттөөгө болот. өзгөрмөлөр. Дал ушул ыкманы австриялык физик Пол Эренфест 1933-жылы фазалык тең салмактуулуктун өзгөрүшү менен болгон бардык белгилүү термодинамикалык процесстердин классификациясын түзгөндө колдонгон.
Термодинамиканын негиздеринен Гиббс энергиясынын температурага карата биринчи туундусу системанын энтропиясынын өзгөрүшүнө барабар экени келип чыгат. Гиббс энергиясынын басымга карата туундусу көлөмдүн өзгөрүшүнө барабар. Эгерде системадагы фазалар өзгөргөндө, энтропия же көлөм үзүлсө, башкача айтканда, алар кескин өзгөрсө, анда алар биринчи тартиптеги фазалык өтүү жөнүндө сөз кылышат.
Мындан ары Гиббс энергиясынын температурага жана басымга карата экинчи туундулары тиешелүүлүгүнө жараша жылуулук сыйымдуулугу жана көлөмдүк кеңейүү коэффициенти болуп саналат. Эгерде фазалардын ортосундагы трансформация көрсөтүлгөн физикалык чоңдуктардын маанилеринин үзгүлтүккө учурашы менен коштолсо, анда экинчи тартиптеги фазалык өтүү жөнүндө сөз болот.
Фазалар ортосундагы трансформациянын мисалдары

Табиятта өтө көп сандагы ар кандай өтүүлөр бар. Бул классификациянын алкагында биринчи түрдөгү өткөөлдөрдүн айкын мисалдары болуп системада көлөмдүн секирүүсүндө металлдарды эрүү процесстери же абадагы суу буусунун конденсацияланышы саналат.
Эгер экинчи тартиптеги өтүүлөр жөнүндө сөз кыла турган болсок, анда эң сонун мисалдар темирдин температурада магниттик абалдан парамагниттик абалга айланышы.768 ºC же абсолюттук нөлгө жакын температурада металл өткөргүчтүн супер өткөргүч абалга айланышы.
Биринчи түрдөгү өтүүлөрдү сүрөттөгөн теңдемелер
Практикада көбүнчө системада фазалык трансформациялар болгондо температуранын, басымдын жана сиңирүү (чыгарылган) энергиянын кандай өзгөрүшүн билүү зарыл. Бул максатта эки маанилүү теңдеме колдонулат. Алар термодинамиканын негиздерин билүүнүн негизинде алынат:
- Клапейрон формуласы, ал ар кандай фазалар арасындагы трансформациялар учурунда басым менен температуранын ортосундагы байланышты белгилейт.
- Сорутуу (чыгарылган) энергия менен системанын температурасын трансформация учурунда байланыштырган Клаузиус формуласы.
Эки теңдемени тең колдонуу физикалык чоңдуктардын сандык көз карандылыктарын алууда гана эмес, фазалык диаграммалардагы тең салмактуулук ийри сызыктарынын жантайышынын белгисин аныктоодо да болуп саналат.
Экинчи түрдөгү өтүүлөрдү сүрөттөө үчүн теңдеме

1-жана 2-түрдөгү фазалык өтүүлөр ар кандай теңдемелер менен сүрөттөлөт, анткени экинчи даражадагы өтүүлөр үчүн Клаузиус жана Клаузиус теңдемелерин колдонуу математикалык белгисиздикке алып келет.
Акыркыны сыпаттоо үчүн Эренфест теңдемелери колдонулат, алар трансформация процессинде жылуулук сыйымдуулугунун жана көлөмдүк кеңейүү коэффициентинин өзгөрүшүн билүү аркылуу басымдын жана температуранын өзгөрүүсүнүн ортосундагы байланышты түзүшөт. Эренфест теңдемелери магнит талаасы жок болгон учурда өткөргүч-өткөргүч өтүүлөрүн сүрөттөө үчүн колдонулат.
Маанилүүлүкфаза диаграммалары
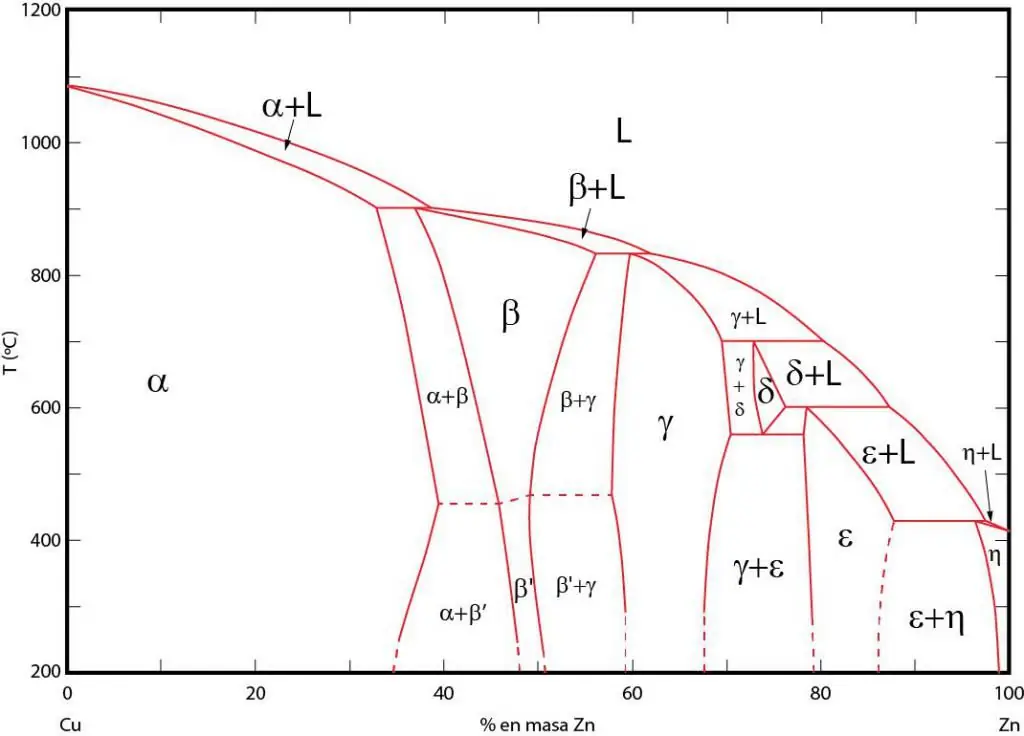
Фаза диаграммалары - бул тиешелүү фазалар тең салмактуулукта болгон аймактардын графикалык көрүнүшү. Бул аймактар фазалардын ортосундагы тең салмактуулук сызыктары менен бөлүнгөн. Көбүнчө P-T (басым-температура), T-V (температура-көлөм) жана P-V (басым-көлөм) фазалык диаграммалары колдонулат.
Фаза диаграммаларынын маанилүүлүгү, алар тышкы шарттар тиешелүү түрдө өзгөргөндө системанын кайсы фазада болоорун алдын ала айтууга мүмкүндүк бергендигинде. Бул маалымат каалаган касиеттерге ээ структураны алуу үчүн ар кандай материалдарды жылуулук менен иштетүүдө колдонулат.






