Физикада термодинамикалык системаларды изилдөөдөгү маанилүү суроолордун бири бул система кандайдыр бир пайдалуу иштерди аткара алабы деген суроо. Иш түшүнүгү менен тыгыз байланыштуу ички энергия түшүнүгү. Бул макалада идеалдуу газдын ички энергиясы эмне экенин карап чыгабыз жана аны эсептөө үчүн формулаларды беребиз.
Идеалдуу газ
Газ жөнүндө, ага тышкы таасир астында эч кандай серпилгичтүү күчкө ээ болбогон жана натыйжада көлөмүн жана формасын сактабаган агрегациялык абал катары ар бир мектеп окуучусу билет. Көптөр үчүн идеалдуу газ түшүнүгү түшүнүксүз жана түшүнүксүз бойдон калууда. Келгиле, түшүндүрүп берели.
Идеал газ - бул төмөнкү эки маанилүү шартты канааттандырган ар кандай газ:
- Аны түзгөн бөлүкчөлөрдүн өлчөмү жок. Алардын өлчөмү бар, бирок алардын ортосундагы аралыкка салыштырмалуу ал ушунчалык кичинекей болгондуктан, бардык математикалык эсептөөлөрдө аны эске албай коюуга болот.
- Бөлүкчөлөр бири-бири менен ван-дер-Ваальс күчтөрүн же күчтөрүн колдонуу менен өз ара аракеттенишпейтбашка жаратылыш. Чынында, бардык реалдуу газдарда мындай өз ара аракеттешүү бар, бирок анын энергиясы кинетикалык бөлүкчөлөрдүн орточо энергиясына салыштырмалуу анча деле чоң эмес.
Сүрөттөлгөн шарттарды дээрлик бардык реалдуу газдар канааттандырат, алардын температурасы 300 Кден жогору, басымдары бир атмосферадан ашпайт. Өтө жогорку басымда жана төмөн температурада газдардын идеалдуу жүрүм-турумунан четтөө байкалат. Бул учурда, бир чыныгы газдар жөнүндө сөз болот. Алар Ван дер Ваальс теңдемеси менен сүрөттөлөт.
Идеалдуу газдын ички энергиясы жөнүндө түшүнүк
Аныктамага ылайык, системанын ички энергиясы бул системанын ичиндеги кинетикалык жана потенциалдык энергиялардын суммасы. Эгерде бул түшүнүк идеалдуу газга карата колдонулса, анда потенциалдуу компоненттен баш тартуу керек. Чынында эле, идеалдуу газдын бөлүкчөлөрү бири-бири менен өз ара аракеттенишпегендиктен, алар абсолюттук вакуумда эркин кыймылдашат деп кароого болот. Изилденип жаткан системадан бир бөлүкчөлөрдү бөлүп алуу үчүн, өз ара аракеттенүүнүн ички күчтөрүнө каршы иштөөнүн кереги жок, анткени бул күчтөр жок.
Ошентип, идеалдуу газдын ички энергиясы дайыма анын кинетикалык энергиясы менен дал келет. Акыркысы, өз кезегинде, системанын бөлүкчөлөрүнүн молярдык массасы, алардын саны, ошондой эле которуу жана айлануу кыймылынын орточо ылдамдыгы менен өзгөчө аныкталат. Кыймыл ылдамдыгы температурага жараша болот. Температуранын жогорулашы ички энергиянын көбөйүшүнө алып келет жана тескерисинче.
Формула үчүнички энергия
Идеал газ системасынын ички энергиясын U тамгасы менен белгилеңиз. Термодинамика боюнча ал системанын H энтальпиясы менен басымдын жана көлөмдүн көбөйтүндүсүнүн ортосундагы айырма катары аныкталат, башкача айтканда:
U=H - pV.
Жогорудагы абзацта биз U-нун мааниси бардык газ бөлүкчөлөрүнүн Ekтолук кинетикалык энергиясына туура келерин аныктадык:
U=Ek.
Статистикалык механикадан идеалдуу газдын молекулярдык-кинетикалык теориясынын (МКТ) алкагында бир бөлүкчөнүн орточо кинетикалык энергиясы Ek1 барабар экени келип чыгат. төмөнкү маани:
Ek1=z/2kBT.
Бул жерде kB жана Т - Больцман туруктуулугу жана температурасы, z - эркиндик даражасынын саны. Ek системасынын жалпы кинетикалык энергиясын Ek1 системадагы N бөлүкчөлөрүнүн санына көбөйтүү аркылуу алууга болот:
Ek=NEk1=z/2NkBT.
Ошентип, идеалдуу газдын ички энергиясынын формуласын алдык, ал абсолюттук температура жана жабык системадагы бөлүкчөлөрдүн саны боюнча жалпы түрдө жазылган:
U=z/2NkBT.
Монатомдуу жана көп атомдуу газ
Макаланын мурунку абзацында жазылган U формуласы аны практикалык колдонуу үчүн ыңгайсыз, анткени N бөлүкчөлөрүнүн санын аныктоо кыйын. Бирок, эгерде n затынын өлчөмүнүн аныктамасын эске алсак, анда бул туюнтманы ыңгайлуураак формада кайра жазууга болот:
n=N/NA; R=NAkB=8, 314 Дж/(молК);
U=z/2nR T.
Эркиндик даражаларынын саны z газды түзгөн бөлүкчөлөрдүн геометриясына көз каранды. Ошентип, бир атомдуу газ үчүн z=3, анткени атом мейкиндиктин үч багытында гана өз алдынча кыймылдай алат. Эгерде газ эки атомдуу болсо, анда z=5, анткени эркиндиктин үч которуу даражасына дагы эки айланма эркиндик даражасы кошулат. Акырында, ар кандай башка көп атомдуу газ үчүн z=6 (3 котормо жана 3 айланма эркиндик даражасы). Ушуну эске алып, бир атомдуу, эки атомдуу жана көп атомдуу идеалдуу газдын ички энергиясынын формулаларын төмөнкү формада жаза алабыз:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Ички энергияны аныктоо тапшырмасынын мисалы
100 литрлик цилиндрде 3 атмосфера басымдагы таза суутек бар. Берилген шарттарда суутек идеалдуу газ деп эсептесек, анын ички энергиясы кандай экенин аныктоо керек.

У үчүн жогорудагы формулалар заттын көлөмүн жана газдын температурасын камтыйт. Маселенин шартында, бул өлчөмдөр жөнүндө таптакыр эч нерсе айтылбайт. Маселени чечүү үчүн универсалдуу Клапейрон-Менделеев теңдемесин эске салуу керек. Ал сүрөттө көрсөтүлгөндөй.
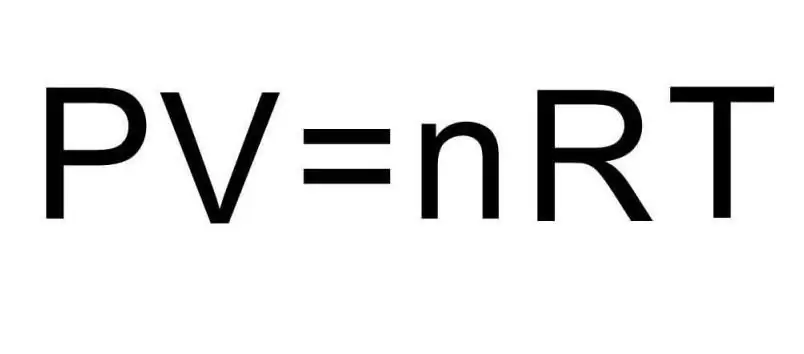
Суутек H2 эки атомдуу молекула болгондуктан, ички энергиянын формуласы:
UH2=5/2nRT.
Эки туюнтманы салыштырып, маселени чечүүнүн акыркы формуласына келебиз:
UH2=5/2PV.
Басым жана көлөм бирдиктерин шарттан SI бирдик системасына айландыруу, UH2 формуласындагы тиешелүү маанилерди алмаштыруу жана жооп: UH2 ≈ 76 кДж.






