Биз жашап жаткан дүйнө элестете алгыс кооз жана жашоонун багытын белгилеген ар кандай процесстерге толгон. Бул процесстердин бардыгын белгилүү илим - физика изилдейт. Бул ааламдын келип чыгышы жөнүндө, жок эле дегенде, кандайдыр бир түшүнүк алууга мүмкүнчүлүк берет. Бул макалада молекулярдык-кинетикалык теория, анын теңдемелери, түрлөрү жана формулалары сыяктуу түшүнүктөрдү карап чыгабыз. Бирок, бул маселелерди тереңирээк изилдөөгө өтүүдөн мурун, физиканын маанисин жана ал изилдеген тармактарды өзүңүзгө тактап алышыңыз керек.
Физика деген эмне?

Чынында, бул абдан кеңири илим жана, балким, адамзат тарыхындагы эң фундаменталдуу илимдин бири. Мисалы, бир эле информатика адам ишинин дээрлик бардык чөйрөсү менен байланышкан болсо, мейли ал эсептөөчү дизайн болобу же мультфильмдерди түзүү болобу, анда физика бул жашоонун өзү, анын татаал процесстеринин жана агымдарынын сүрөттөлүшү. Келгиле, анын маанисин мүмкүн болушунча жөнөкөйлөштүрүүгө аракет кылалы.
ОшентипОшентип, физика энергия менен материяны, алардын ортосундагы байланыштарды изилдөө, биздин кең ааламда болуп жаткан көптөгөн процесстерди түшүндүрүү менен алектенген илим. Заттын түзүлүшүнүн молекулярдык-кинетикалык теориясы физиканын теорияларынын жана тармактарынын деңизиндеги кичинекей бир тамчы гана.
Бул илим майда-чүйдөсүнө чейин изилдеген энергия ар кандай формада көрсөтүлүшү мүмкүн. Мисалы, жарык, кыймыл, тартылуу, радиация, электр жана башка көптөгөн формаларда. Биз бул макалада бул формалардын түзүлүшүнүн молекулярдык-кинетикалык теориясына токтолобуз.
Материяны изилдөө бизге заттын атомдук түзүлүшү жөнүндө түшүнүк берет. Айтмакчы, ал молекулярдык-кинетикалык теориядан келип чыгат. Заттын түзүлүшү жөнүндөгү илим бизге жашообуздун маанисин, жашоонун жана Ааламдын пайда болушунун себептерин түшүнүүгө жана табууга мүмкүндүк берет. Келгиле, дагы эле заттын молекулярдык-кинетикалык теориясын изилдөөгө аракет кылалы.
Биринчиден, терминологияны жана бардык корутундуларды толук түшүнүү үчүн бир аз киришүү керек.
Физика темалары
Молекулярдык-кинетикалык теория эмне деген суроого жооп берип жатып, физиканын бөлүмдөрү жөнүндө айтпай коюуга болбойт. Булардын ар бири адам жашоосунун белгилүү бир тармагын деталдуу изилдөө жана түшүндүрүү менен алектенет. Алар төмөнкүдөй классификацияланат:
- Механика, ал дагы эки бөлүккө бөлүнгөн: кинематика жана динамика.
- Статикалык.
- Термодинамика.
- Молекулярдык бөлүм.
- Электродинамика.
- Оптика.
- Кванттардын физикасы жана атомдук ядро.
Келгиле, өзгөчө молекулярдык жөнүндө сүйлөшөлүфизика, анткени ал молекулярдык-кинетикалык теорияга негизделген.
Термодинамика деген эмне?
Жалпысынан молекулярдык бөлүк жана термодинамика физиканын физикалык системалардын жалпы санынын макроскопиялык компонентин гана изилдеген тыгыз байланышкан тармактары болуп саналат. Бул илимдер денелердин жана заттардын ички абалын так сүрөттөй турганын эстен чыгарбоо керек. Мисалы, алардын ысытуу, кристаллдашуу, буулануу жана конденсация учурундагы абалы, атомдук деңгээлде. Башкача айтканда, молекулярдык физика - бул өтө көп сандагы бөлүкчөлөрдөн: атомдордон жана молекулалардан турган системалар жөнүндөгү илим.
Молекулярдык-кинетикалык теориянын негизги жоболорун ушул илимдер изилдеген.
Жетинчи класстын курсунда да микро жана макродүйнө, система деген түшүнүктөр менен тааныштык. Бул терминдерди эс тутумга жаңылоо ашыкча болбойт.
Микродүйнө, анын атынан көрүнүп тургандай, элементардык бөлүкчөлөрдөн турат. Башкача айтканда, бул кичинекей бөлүкчөлөр дүйнөсү. Алардын өлчөмдөрү 10-18 мден 10-4 мге чейинки диапазондо өлчөнөт жана алардын чыныгы абалынын убактысы чексиздикке да, чексиздикке да жетиши мүмкүн. пропорционалдуу эмес кичинекей интервалдар, мисалы, 10-20 s.
Macroworld көптөгөн элементардык бөлүкчөлөрдөн турган туруктуу формадагы денелерди жана системаларды карайт. Мындай системалар адамдык көлөмүбүзгө дал келет.
Мындан тышкары, мега дүйнө деген нерсе бар. Ал чоң планеталардан, космостук галактикалардан жана комплекстерден турат.
Негиздертеория
Эми биз бир аз кайталап жана физиканын негизги терминдерин эстеп калгандан кийин, бул макаланын негизги темасына түз өтсөк болот.
Молекулярдык-кинетикалык теория пайда болгон жана биринчи жолу XIX кылымда түзүлгөн. Анын маңызы Роберт Гук, Исаак сыяктуу көрүнүктүү илимпоздордун божомолдорунан чогултулган үч фундаменталдык жобонун негизинде кандайдыр бир заттын түзүлүшүн (көбүнчө катуу жана суюк денелерге караганда газдардын түзүлүшүн) деталдуу түрдө сүрөттөп бергенинде. Ньютон, Даниел Бернулли, Михаил Ломоносов жана башкалар.
Молекулярдык-кинетикалык теориянын негизги жоболору мындай угулат:
- Бардык заттар (алар суюк, катуу же газ абалына карабастан) майда бөлүкчөлөрдөн: молекулалардан жана атомдордон турган татаал түзүлүшкө ээ. Атомдорду кээде "элементардык молекулалар" деп да коюшат.
- Бул элементардык бөлүкчөлөрдүн баары дайыма үзгүлтүксүз жана башаламан кыймыл абалында болушат. Ар бирибиз бул сунуштун тике далилине туш болдук, бирок, кыязы, ага анча маани берген жокпуз. Мисалы, күн нурларынын фонунда чаң бөлүкчөлөрү тынымсыз башаламан багытта жылып жатканын баарыбыз көрдүк. Мунун себеби атомдор бири-бирине тынымсыз кинетикалык энергия берип, бири-бири менен өз ара түртүп чыгышат. Бул кубулуш биринчи жолу 1827-жылы изилденген жана ал ачуучунун атынан аталган - "Браун кыймылы".
- Бардык элементардык бөлүкчөлөр бири-бири менен үзгүлтүксүз өз ара аракеттенүү процессиндеэлектрдик текке ээ болгон кээ бир күчтөр.
Экинчи позицияны сүрөттөгөн дагы бир мисал, мисалы, газдардын молекулярдык-кинетикалык теориясына да тиешелүү болушу мүмкүн, бул диффузия экенин белгилей кетүү керек. Биз аны күнүмдүк жашоодо жана бир нече сыноолордо жана контролдоодо жолуктурабыз, андыктан бул тууралуу түшүнүккө ээ болуу маанилүү.
Биринчи, төмөнкү мисалдарды карап көрөлү:
Дарыгер кокусунан столдун үстүндөгү колбадан спирт төгүп алган. Же атырдын бөтөлкөңүздү жерге түшүрүп алсаңыз, ал бүт жерге тарап кеткендир.
Эмне үчүн бул эки учурда спирттин жыты да, атырдын жыты да бир канча убакыттан кийин бул заттардын ичиндегилер төгүлгөн жерди эле эмес, бүт бөлмөнү толтурат?
Жообу жөнөкөй: диффузия.
Диффузия - бул эмне? Ал кантип агып жатат?

Бул белгилүү бир затты түзгөн бөлүкчөлөрдүн (көбүнчө газ) башкасынын молекулалар аралык боштуктарына кирүү процесси. Жогорудагы мисалдарыбызда төмөнкүдөй болгон: термикалык, б.а. үзгүлтүксүз жана диссоциацияланган кыймылдан улам аба молекулаларынын ортосундагы боштуктарга спирт жана/же атыр молекулалары түшкөн. Бара-бара, абанын атомдору жана молекулалары менен кагылышуунун таасири астында, алар бөлмөнүн айланасына тарады. Айтмакчы, диффузиянын интенсивдүүлүгү, башкача айтканда анын агымынын ылдамдыгы диффузияга катышкан заттардын тыгыздыгына, ошондой эле кинетикалык деп аталган алардын атомдору менен молекулаларынын кыймыл энергиясына көз каранды. Кинетикалык энергия канчалык чоң болсо, бул молекулалардын ылдамдыгы жана интенсивдүүлүгү ошончолук жогору болот.
Эң ылдам диффузия процессин газдардагы диффузия деп атоого болот. Бул газ өзүнүн курамы боюнча бир тектүү эмес экендигине байланыштуу, бул газдардагы молекулалар аралык боштуктар тиешелүүлүгүнө жараша олуттуу көлөмдөгү мейкиндикти ээлейт жана аларга бөтөн заттын атомдору менен молекулаларын алуу процесси оңой жана тез жүрөт..
Бул процесс суюктуктарда бир аз жайыраак. Бир кружка чайда кант кубиктеринин эриши катуу заттын суюктуктагы диффузиясынын мисалы гана.
Бирок эң узун убакыт бул катуу кристаллдык түзүлүштөгү денелердеги диффузия. Бул так ошондой, анткени катуу заттардын түзүлүшү бир тектүү жана күчтүү кристалл торчосуна ээ, анын клеткаларында катуу заттын атомдору титирет. Мисалы, эки металл тилкенин беттери жакшылап тазаланып, анан бири-бирине тийип калса, анда жетиштүү убакыт өткөндөн кийин биз бир металлдын экинчи металлдын бөлүктөрүн аныктай алабыз жана тескерисинче.
Башка фундаменталдуу бөлүмдөр сыяктуу эле физиканын негизги теориясы да өзүнчө бөлүктөргө бөлүнөт: классификация, типтер, формулалар, теңдемелер ж.б. Ошентип, биз молекулярдык кинетикалык теориянын негиздерин үйрөндүк. Бул жеке теориялык блокторду кароого коопсуз өтсөңүз болот дегенди билдирет.
Газдардын молекулярдык-кинетикалык теориясы
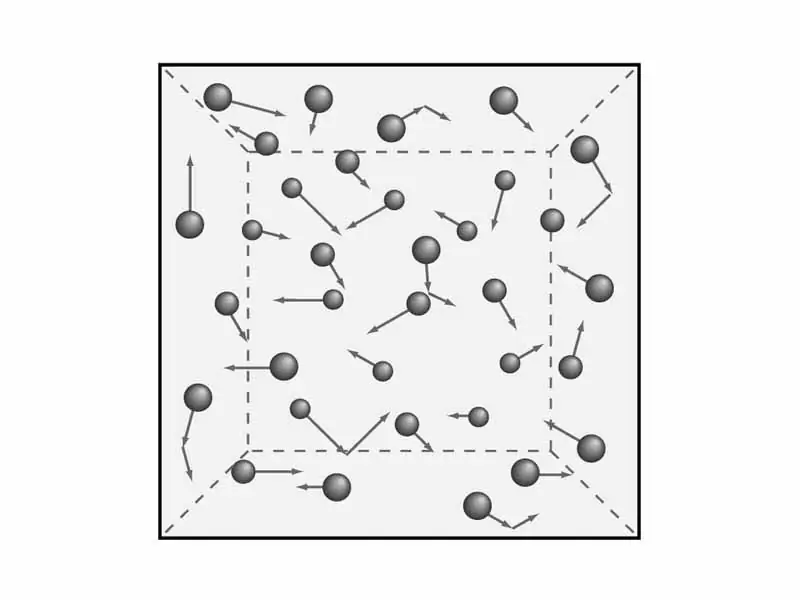
Газ теориясынын жоболорун түшүнүү зарыл. Жогоруда айтылгандай, газдардын басым жана температура сыяктуу макроскопиялык мүнөздөмөлөрүн карап чыгабыз. Булгаздардын молекулярдык-кинетикалык теориясынын теңдемесин чыгаруу үчүн кийинчерээк керек болот. Ал эми математика - кийинчерээк, эми теорияны жана ошого жараша физиканы карайлы.
Окумуштуулар газдардын кинетикалык моделин түшүнүүгө кызмат кылган газдардын молекулалык теориясынын беш жобосун түзүшкөн. Алар мындай угулат:
- Бардык газдар белгилүү бир чоңдугу жок, бирок белгилүү бир массасы бар элементардык бөлүкчөлөрдөн турат. Башкача айтканда, бул бөлүкчөлөрдүн көлөмү алардын ортосундагы узундукка салыштырмалуу минималдуу.
- Газдардын атомдору жана молекулалары иш жүзүндө потенциалдуу энергияга ээ эмес, тиешелүүлүгүнө жараша мыйзамга ылайык, бардык энергия кинетикалык энергияга барабар.
- Бул позиция менен мурда таанышканбыз - Броун кыймылы. Башкача айтканда, газ бөлүкчөлөрү дайыма үзгүлтүксүз жана башаламан кыймылда болушат.
- Тезинен ылдамдык жана энергия кабары менен коштолгон газ бөлүкчөлөрүнүн бардык өз ара кагылышуулары толугу менен ийкемдүү. Бул кагылышуу учурунда алардын кинетикалык энергиясында эч кандай энергия жоготуу же кескин секирүү болбойт дегенди билдирет.
- Кадимки шарттарда жана туруктуу температурада дээрлик бардык газдардын бөлүкчөлөрүнүн кыймылынын орточо энергиясы бирдей.
Газдардын молекулярдык-кинетикалык теориясынын теңдемесинин ушул түрү аркылуу бешинчи позицияны кайра жаза алабыз:
E=1/2mv^2=3/2kT, мында k - Больцман туруктуусу; T - Кельвиндеги температура.
Бул теңдеме газдын элементардык бөлүкчөлөрүнүн ылдамдыгы менен алардын абсолюттук температурасынын ортосундагы байланышты түшүнүүгө жардам берет. Демек, алардын абсолюттук жогорутемпература, алардын ылдамдыгы жана кинетикалык энергиясы ошончолук чоң болот.
Газ басымы
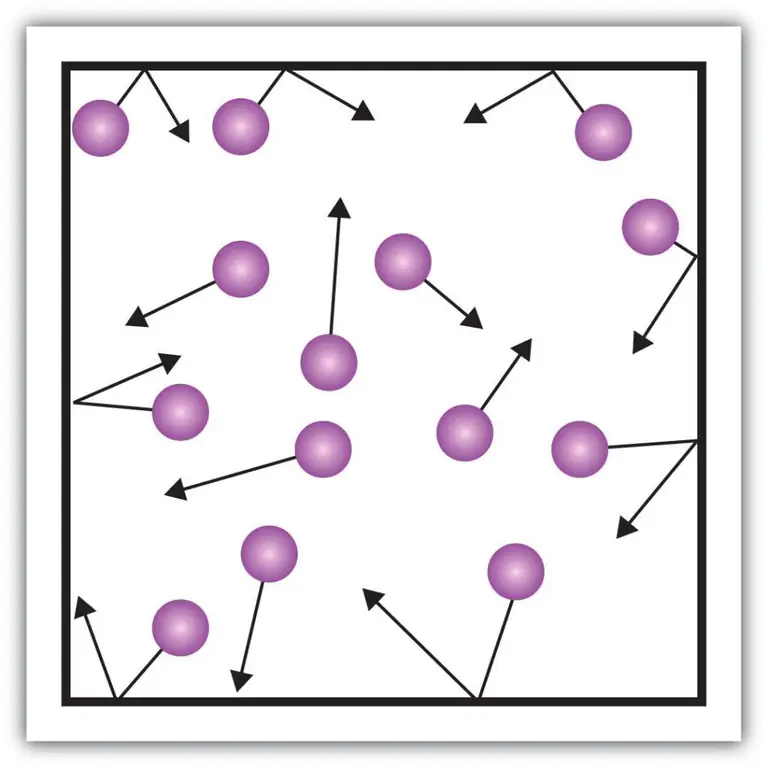
Мүнөздөөнүн мындай макроскопиялык компоненттери, мисалы, газдардын басымы, кинетикалык теорияны колдонуу менен да түшүндүрүүгө болот. Бул үчүн, келгиле, төмөнкү мисалды элестетип көрөлү.
Келгиле, кандайдыр бир газдын молекуласы кутучанын ичинде деп алалы, анын узундугу L. Жогоруда сүрөттөлгөн газ теориясынын жоболорун колдонуп, молекулалык сфера х боюнча гана кыймылдаарын эске алалы. -ок. Ошентип, биз идиш (куту) дубалдарынын бири менен серпилгичтүү кагылышуу процессин байкай алабыз.
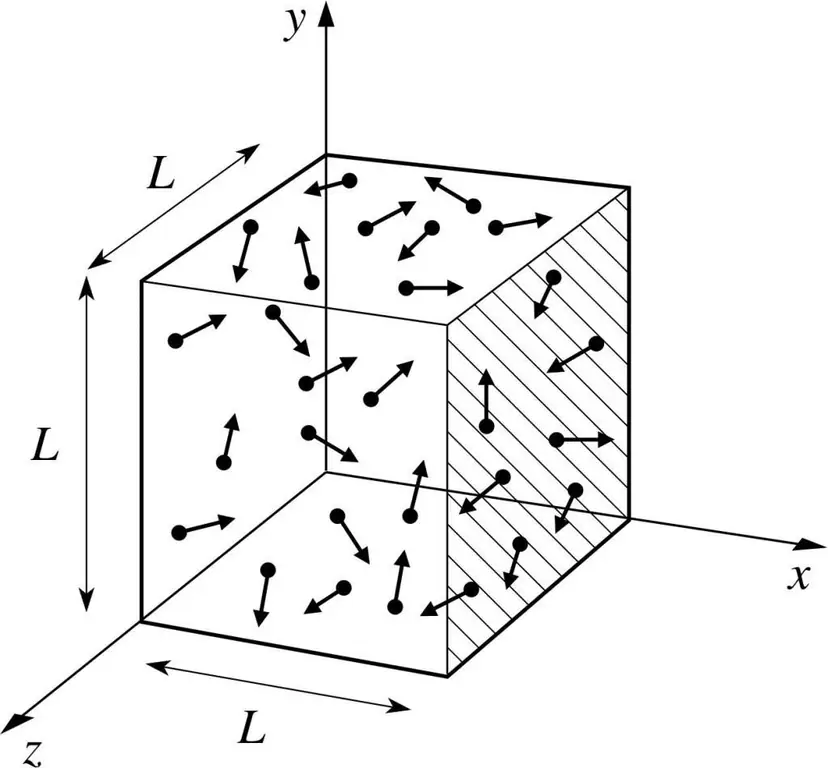
Учурдагы кагылышуунун импульсу, биз билгендей, формула менен аныкталат: p=mv, бирок бул учурда бул формула проекциялык форманы алат: p=mv(x).
Х огунун өлчөмүн, башкача айтканда, х огун гана карагандыктан, импульстун жалпы өзгөрүүсү төмөнкү формула менен туюнат: mv(x) - m(-v() x))=2mv(x).
Кийин, Ньютондун экинчи мыйзамын колдонуу менен объектибиз көрсөткөн күчтү карап көрөлү: F=ma=P/t.
Бул формулалардан газ тараптан басымды туюндуруп алабыз: P=F/a;
Эми келип чыккан формулага күч туюнтмасын алмаштырып, алалы: P=mv(x)^2/L^3.
Андан кийин биздин даяр басым формулабыз газ молекулаларынын N-саны үчүн жазылышы мүмкүн. Башкача айтканда, мындай болот:
P=Nmv(x)^2/V, мында v - ылдамдык жана V - көлөм.
Эми газ басымы боюнча бир нече негизги жоболорду бөлүп көрсөтүүгө аракет кылалы:
- Бул аркылуу көрүнөтал жайгашкан объекттин дубалдарынын молекулалары менен молекулалардын кагылышуусу.
- Басымдын чоңдугу молекулалардын идиштин дубалдарына тийгизген таасиринин күчүнө жана ылдамдыгына түз пропорционалдуу.
Теория боюнча кээ бир кыскача корутундулар
Молекулярдык-кинетикалык теориянын негизги теңдемесин карап чыгуудан мурун, биз сизге жогорудагы пункттардан жана теориядан бир нече кыскача корутундуларды сунуштайбыз:
- Атомдорунун жана молекулаларынын кыймылынын орточо энергиясынын өлчөмү абсолюттук температура болуп саналат.
- Эки башка газ бирдей температурада болгондо, алардын молекулаларынын орточо кинетикалык энергиясы бирдей болот.
- Газ бөлүкчөлөрүнүн энергиясы орточо квадраттык ылдамдыкка түз пропорционал: E=1/2mv^2.
- Газ молекулаларынын орточо кинетикалык энергиясы жана орточо ылдамдыгы бар болгону менен, айрым бөлүкчөлөр ар кандай ылдамдыкта кыймылдайт: кээ бирлери тез, кээ бири жай.
- Температура канчалык жогору болсо, молекулалардын ылдамдыгы ошончолук жогору болот.
- Газдын температурасын канча эсе көтөрсөк (мисалы, эки эсе), анын бөлүкчөлөрүнүн кыймыл энергиясы ошончо эсе көбөйөт (тиешелүүлүгүнө жараша эки эсе көбөйөт).
Негизги теңдеме жана формулалар

Молекулярдык-кинетикалык теориянын негизги теңдемеси микродүйнөнүн чоңдуктары менен ошого жараша макроскопиялык, башкача айтканда өлчөнгөн чоңдуктардын ортосундагы байланышты түзүүгө мүмкүндүк берет.
Молекулярдык теория карап чыга турган эң жөнөкөй моделдердин бири - идеалдуу газ модели.
Ошентип айтса болотбул идеалдуу газдын молекулярдык кинетикалык теориясы тарабынан изилденген ойдон чыгарылган моделдин бир түрү, мында:
- жөнөкөй газ бөлүкчөлөрү бири-бири менен да, кандайдыр бир идиштердин дубалдарынын молекулалары менен да өз ара аракеттенүүчү, бир гана учурда - абсолюттук серпилгичтүү кагылышууда кемчиликсиз ийкемдүү шарлар катары каралат;
- газдын ичинде тартылуу күчтөрү жок, же алар чындыгында этибарга алынбай калышы мүмкүн;
- материалдык чекиттер катары газдын ички түзүлүшүнүн элементтерин алууга болот, башкача айтканда, алардын көлөмүн да эске албай коюуга болот.
Мындай моделди карап, немецтик физик Рудольф Клаузиус микро жана макроскопиялык параметрлердин байланышы аркылуу газ басымынын формуласын жазган. Төмөнкүдөй көрүнөт:
p=1/3m(0)nv^2.
Кийинчерээк бул формула идеалдуу газдын молекулярдык-кинетикалык теориясынын негизги теңдемеси деп аталат. Ал бир нече түрдүү формада берилиши мүмкүн. Эми биздин милдетибиз молекулярдык физика, молекулярдык кинетикалык теория сыяктуу бөлүмдөрдү, демек, алардын толук теңдемелерин жана түрлөрүн көрсөтүү. Ошондуктан, негизги формуланын башка вариацияларын карап чыгуунун мааниси бар.
Газ молекулаларынын кыймылын мүнөздөгөн орточо энергияны төмөнкү формула аркылуу табууга болорун билебиз: E=m(0)v^2/2.
Мындай учурда баштапкы басым формуласындагы m(0)v^2 туюнтмасын орточо кинетикалык энергия менен алмаштырсак болот. Мунун натыйжасында газдардын молекулярдык-кинетикалык теориясынын негизги теңдемесин төмөнкү формада түзүүгө мүмкүнчүлүк алабыз: p=2/3nE.
Мындан тышкары, m(0)n туюнтмасын эки бөлүктүн көбөйтүндүсү катары жазууга болорун баарыбыз билебиз:
m/NN/V=m/V=ρ.
Бул манипуляциялардан кийин идеалдуу газдын молекулярдык-кинетикалык теориясынын теңдемеси үчүн формулабызды үчүнчү, башкача түрдө кайра жаза алабыз:
p=1/3ρv^2.
Ооба, балким, бул тема боюнча билишиңиз керек болгон нерсе. Алган билимдерди кыскача (андай эмес) корутундулар түрүндө системалаштыруу гана калды.
"Молекулярдык-кинетикалык теория" темасындагы бардык жалпы корутундулар жана формулалар
Келиңиз баштайлы.
Биринчи:
Физика - табият таануу курсуна кирген фундаменталдык илим, ал заттын жана энергиянын касиеттерин, алардын түзүлүшүн, органикалык эмес табияттын мыйзам ченемдүүлүктөрүн изилдейт.
Ал төмөнкү бөлүмдөрдү камтыйт:
- механика (кинематика жана динамика);
- статикалык;
- термодинамика;
- электродинамика;
- молекулярдык бөлүм;
- оптика;
- кванттардын физикасы жана атомдук ядро.
Экинчи:
Бөлүкчөлөр физикасы жана термодинамика физикалык системалардын жалпы санынын макроскопиялык компонентин, башкача айтканда, эбегейсиз сандагы элементардык бөлүкчөлөрдөн турган системаларды изилдеген бири-бири менен тыгыз байланышкан тармактар.
Алар молекулярдык-кинетикалык теорияга негизделген.
Үчүнчү:
Маселенин өзөгү мына ушунда. Молекулярдык-кинетикалык теория заттын түзүлүшүн (катуу заттарга караганда көбүнчө газдардын түзүлүшүн) кеңири сүрөттөйт.жана суюк денелер), көрүнүктүү окумуштуулардын божомолдорунан чогултулган үч фундаменталдуу божомолдорго негизделген. Алардын арасында: Роберт Гук, Исаак Ньютон, Даниел Бернулли, Михаил Ломоносов жана башкалар.
Төртүнчүсү:
Молекулярдык-кинетикалык теориянын үч негизги жобосу:
- Бардык заттар (суюк, катуу же газ абалына карабастан) майда бөлүкчөлөрдөн: молекулалардан жана атомдордон турган татаал түзүлүшкө ээ.
- Бул жөнөкөй бөлүкчөлөрдүн баары тынымсыз башаламан кыймылда. Мисал: Броун кыймылы жана диффузиясы.
- Бардык молекулалар кандайдыр бир шарттарда бири-бири менен электр тектерине ээ болгон белгилүү бир күчтөр менен өз ара аракеттенишет.
Молекулярдык-кинетикалык теориянын бул жоболорунун ар бири заттын түзүлүшүн изилдөөдө бекем негиз болуп саналат.
Бешинчиси:
Газ модели үчүн молекулярдык теориянын бир нече негизги пункттары:
- Бардык газдар белгилүү бир чоңдугу жок, бирок белгилүү бир массасы бар элементардык бөлүкчөлөрдөн турат. Башкача айтканда, бул бөлүкчөлөрдүн көлөмү алардын ортосундагы аралыктарга салыштырмалуу минималдуу.
- Газдардын атомдору жана молекулалары иш жүзүндө потенциалдуу энергияга ээ эмес, алардын жалпы энергиясы кинетикалык энергияга барабар.
- Бул позиция менен мурда таанышканбыз - Броун кыймылы. Башкача айтканда, газ бөлүкчөлөрү дайыма үзгүлтүксүз жана туш келди кыймылда болот.
- Атомдордун жана газдардын молекулаларынын ылдамдык жана энергия билдирүүсү менен коштолгон бардык өз ара кагылышуулары толугу менен ийкемдүү. Булкагылышуу учурунда алардын кинетикалык энергиясында эч кандай энергия жоготуу же кескин секирүү болбойт дегенди билдирет.
- Кадимки шарттарда жана туруктуу температурада дээрлик бардык газдардын орточо кинетикалык энергиясы бирдей.
Алтынчы:
Газдар боюнча теориянын корутундулары:
- Абсолюттук температура анын атомдорунун жана молекулаларынын орточо кинетикалык энергиясынын өлчөмү.
- Эки башка газ бирдей температурада болгондо, алардын молекулаларынын орточо кинетикалык энергиясы бирдей болот.
- Газ бөлүкчөлөрүнүн орточо кинетикалык энергиясы орточо квадраттык ылдамдыкка түз пропорционал: E=1/2mv^2.
- Газ молекулаларынын орточо кинетикалык энергиясы жана орточо ылдамдыгы бар болгону менен, айрым бөлүкчөлөр ар кандай ылдамдыкта кыймылдайт: кээ бирлери тез, кээ бири жай.
- Температура канчалык жогору болсо, молекулалардын ылдамдыгы ошончолук жогору болот.
- Газдын температурасын канча жолу көтөрсөк (мисалы, эки эсе), анын бөлүкчөлөрүнүн орточо кинетикалык энергиясы да ушунча эсе көбөйөт (тиешелүүлүгүнө жараша эки эсе көбөйөт).
- Газдын ал жайгашкан идиштин дубалдарына болгон басымы менен молекулалардын бул дубалдарга тийгизген таасиринин интенсивдүүлүгүнүн ортосундагы байланыш түз пропорционалдуу: таасир канчалык көп болсо, басым ошончолук жогору болот жана тескерисинче.
Жетинчи:
Идеалдуу газ модели - бул төмөнкү шарттар аткарылышы керек болгон модел:
- Газ молекулалары кемчиликсиз серпилгич шарлар катары каралат.
- Бул шарлар бири-бири менен жана каалаганынын дубалдары менен иштеше алатидиш бир гана учурда - толук ийкемдүү кагылышуу.
- Газдын атомдору менен молекулаларынын ортосундагы өз ара аракетти сүрөттөгөн күчтөр жок же чындыгында көңүл бурбай коюуга болот.
- Атомдор жана молекулалар материалдык чекиттер катары каралат, башкача айтканда, алардын көлөмүн да эске албай коюуга болот.
Сегизинчи:
Бардык негизги теңдемелерди берели жана «Молекулярдык-кинетикалык теория» темасындагы формулаларды көрсөтөлү:
p=1/3m(0)nv^2 - идеалдуу газ моделинин негизги теңдемеси, немис физиги Рудольф Клаузиус тарабынан алынган.
p=2/3nE - идеалдуу газдын молекулярдык-кинетикалык теориясынын негизги теңдемеси. Молекулалардын орточо кинетикалык энергиясынан алынган.
р=1/3ρv^2 - ошол эле теңдеме, бирок идеалдуу газ молекулаларынын тыгыздыгы жана орточо квадраттык ылдамдыгы аркылуу каралат.
m(0)=M/N(a) - Авогадро саны аркылуу бир молекуланын массасын табуу формуласы.
v^2=(v(1)+v(2)+v(3)+…)/N - молекулалардын орточо квадраттык ылдамдыгын табуу формуласы, мында v(1), v(2), v (3) жана башкалар - биринчи молекуланын ылдамдыгы, экинчи, үчүнчү жана башкалар n-молекулага чейин.
n=N/V - молекулалардын концентрациясын табуу формуласы, мында N - берилген V көлөмдөгү газ көлөмүндөгү молекулалардын саны.
E=mv^2/2=3/2kT - молекулалардын орточо кинетикалык энергиясын табуу формулалары, мында v^2 - молекулалардын орточо квадраттык ылдамдыгы, k - туруктуу Людвиг Больцмандын физикасы Австриянын атынан аталган маани, ал эми T газдын температурасы.
p=nkT - концентрация боюнча басым формуласы, туруктууБольцман жана абсолюттук температура Т. Андан орус окумуштуусу Менделеев жана француз физик-инженери Клайперон ачкан дагы бир фундаменталдуу формула келип чыгат:
pV=m/MRT, мында R=kN(a) газдар үчүн универсалдуу константа.
Эми ар кандай изо-процесстер үчүн константаларды көрсөтөлү: изобардык, изохоралык, изотермиялык жана адиабаттык.
pV/T=const - газдын массасы жана курамы туруктуу болгондо аткарылат.
рV=const - эгерде температура да туруктуу болсо.
V/T=const - эгерде газ басымы туруктуу болсо.
p/T=const - үнү туруктуу болсо.
Балким, бул тема боюнча билишиңиз керек болгон нерсе.
Бүгүн биз теориялык физика, анын бир нече бөлүмдөрү жана блоктору сыяктуу илимий тармакка кирдик. Кененирээк, биз физиканын фундаменталдык молекулярдык физика жана термодинамика сыяктуу чөйрөсүнө, тактап айтканда, молекулалык-кинетикалык теорияга токтолдук, ал алгачкы изилдөөдө эч кандай кыйынчылыктарды туудурбайт, бирок чындыгында көптөгөн тузактар бар.. Бул идеалдуу газ модели жөнүндөгү түшүнүгүбүздү кеңейтет, аны биз да кылдат изилдеп чыктык. Кошумчалай кетсек, биз молекулалык теориянын негизги теңдемелери менен алардын ар түрдүү вариациялары менен таанышканыбызды, ошондой эле бул тема боюнча белгилүү бир белгисиз чоңдуктарды табуу үчүн эң керектүү формулалардын баарын карап чыкканыбызды белгилей кетүү керек. Бул жазууга даярданууда өзгөчө пайдалуу болот. ар кандай тесттер, сынактар жана тесттер, же физика боюнча жалпы көз карашты жана билимди кеңейтүү үчүн.
Бул макала сиз үчүн пайдалуу болду деп үмүттөнөбүз жана сиз андан эң керектүү маалыматты гана алып, молекулярдык кинетикалык теориянын негизги жоболору сыяктуу термодинамиканын түркүктөрүндөгү билимиңизди бекемдиңиз.






